Заказ OnLine : Ваша корзина
Биологический молекулярный мотор, управляемый светом
Молекулярные моторы лежат в основе движения биологических систем. Молекулярные моторы управляют движением компонентов клетки, целых клеток и даже сокращением мышц.
Группа исследователей из Массачусетского технологического института и Университета Вирджинии смогли дополнить молекулярный мотор миозин «переключателем», который активируется действием света. Как сообщают исследователи, новая разработка позволит отслеживать в реальном времени внутриклеточные процессы, протекающие с участием миозина.
Для сокращения мышц необходимо взаимодействие двух нитевидных белков – миозина и актина. Управляемые расщеплением внутриклеточного «топлива» – аденозинтрифосфата (АТФ) определенные домены молекулы миозина связываются с нитями актина. В клетках, не образующих мышечную ткань, миозин контролирует процессы, связанные с процессом клеточного деления.
Миозин состоит из нескольких различных белковых цепей. Активность миозина, не входящего в состав мышечной ткани, управляется его регуляторной легкой цепью. После связывания фосфатной группы с определенным фрагментом регуляторной цепи (Ser19) миозин активируется. Активность белка может быть повышена за счет фосфорилирования располагающегося рядом аминокислотного остатка (Thr18).
Миозин является объектом интенсивного обучения, однако до настоящего времени не было точно обнаружено, какие процессы протекают в живых клетках сразу непосредственно после активации и спустя некоторое время после нее.
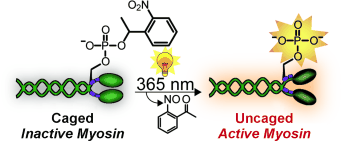
Исследователи, работавшие под руководством Империали, разработали метод, позволяющий проводить наблюдение процессов, протекающих с участием миозина – они получили молекулу миозина, которая может управляться действием света. Для этого исследователи получили синтетическую регуляторную цепь белка, уже содержащую одну или две фосфатные группы, одна из которых была инкапсулирована в молекулярную клетку. Цепь, содержащая инкапсулированный фосфатный фрагмент, неактивна, однако при облучении клетка-капсула расщепляется, что «включает» регуляторную цепь и активирует миозин.
Исследователи заменили нативную регуляторную цепь миозина на синтетическую, после чего ввели полученный миозин, активируемый светом, непосредственно в клетки, добившись того, чтобы облучение света активировала миозин в нужное время и в нужном месте. Исследователи полагают, что такой подход позволит им наблюдать, что происходит с активированным миозином в клетке в режиме реального времени.











