Заказ OnLine : Ваша корзина
Наноалмазы для борьбы с раком
Наночастицы с большим количеством граней, построенные по типу огранённых драгоценных камней могут не только доставлять лекарственные препараты в клетки опухоли, но и обеспечить, чтобы молекулы равномерно распределялись по поверхности граней такой наночастицы, чтобы за счет увеличения своей площади поверхности достичь максимального терапевтического эффекта.
Неудачи химиотерапии связаны во много с тем, что часто клетки защищают себя, выталкивая из себя чужеродные соединения за счет работы белков-переносчиков. Такая естественная защита клеток приводит к тому, что для эффективности лечения лечащим врачам приходится значительно увеличивать концентрации препаратов, однако помимо усиления терапевтического эффекта увеличение концентрации препаратов для химиотерапии значительно повышает риск развития побочных эффектов.
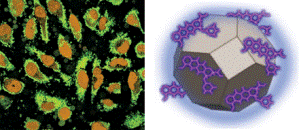
Флуоресцентная спектроскопия показывает, что наноалмазы (зеленые), с «полезной нагрузкой» из доксорубицина (схематичное представление на правой схеме) могут усваиваться клетками линии HeLa (ядра клеток оранжевые), размер которых обычно составляет 20-30 мкм.
Наночастицы не могут быть отторгаемы клетками так быстро, при этом с наночастицами может быть связано большое количество низкомолекулярных соединений – все это обуславливает перспективность применения наночастиц в качестве систем для переноски лекарственных препаратов. Особо пристальное внимание исследователей привлекают наноалмазы с размерами от 2 до 8 нанометров – по словам Дина Хо такие частицы обладают уникальными электростатическими свойствами, способствующими связыванию с ними лекарственного препарата для химиотерапии.
Связывание противоракового препарата доксорубицина (doxorubicin) позволило исследователям из группы Хо провести доставку лекарственного препарата в различные опухолевые клетки мышей. Независимо от того, какой тип ткани был поражено злокачественными образованиями, через семь дней после инъекции наноалмазы с «полезной нагрузкой» из противораковых препаратов уничтожили втрое больше опухолевых клеток, чем доксорубицин, введенный в опухолевые ткани контрольной группы животных. Системы наноалмазы/доксорубицин циркулировали в кровеносной системе мышей в 10 раз дольше, чем доксорубицин, который не был связан ни с чем.
При введении подопытным мышам высокой дозы доксорубицина (200 мкг) мыши, пораженные опухолями молочных желез, умирали через 15 дней после инъекции. Однако для мышей, лечение которых проводилось эквивалентными дозами комплекса наноалмаз/доксорубицин, выживаемость в течение 8 недель составляла почти 100%, а размеры опухоли уменьшались примерно на 50%.











